RHU DESTINATION 2024 : un projet grandi par ses dynamiques évolutives

Le 11 mars 2026, le Siège de l’AP-HP a accueilli l’ensemble les parties prenantes du programme de recherche hospitalo-universitaire (RHU) en santé DESTINATION 2024 : dépistage, évaluation et traitement de l’hypertension pulmonaire thromboembolique chronique (HTP-TEC). Retour sur six années de collaboration, d’adaptation et d’engagement partagé.
Le Pr Marc Humbert, responsable scientifique du RHU DESTINATION 2024, a introduit la journée de bilan de ce projet d’innovation, par et pour la recherche, lancé pendant la crise Covid en 2020. Un projet accompagné par les patients, les hospitaliers, universitaires, organismes de recherche et les partenaires industriels : Actelion (Janssen Pharmaceutical Companies of Johnson & Johnson) et GE HealthCare.
« Quand on parle d’hypertension pulmonaire, on parle d’une élévation chronique de la pression dans les artères pulmonaires », l’objectif est alors de diagnostiquer avec certitude la maladie : estimation de la pression élevée par échographie cardiaque et certitude par une mesure invasive des pressions par cathétérisme cardiaque droit pratiqué dans des centres experts. Ensuite, il faut déterminer si cela est pré ou postcapillaire (maladie du cœur ou des artères pulmonaires) et les mécanismes sous-jacents impliqués pour adapter les interventions thérapeutiques. Au lancement de ce projet, en 2018, l’hypertension pulmonaire thromboembolique chronique était complexe car elle nécessitait une approche multidisciplinaire (ingénieurs, médecins, chirurgiens, radiologues, industries, chercheurs). Ainsi, le volume de prise en charge permet l’expertise ce d’autant plus qu’il n’existe pas d’opposition des stratégies mais bien une combinaison des stratégies de traitements (médicamenteux, angioplastie, chirurgie) pour les patients.
Ces sept dernières années, l’évolution dans ce domaine a été forte, ainsi l’HTP-TEC doit pouvoir être traitée de manière efficace chez les patients avec une résolution du risque mortel. Elle est la conséquence de séquelles d’embolies pulmonaires (35000 cas/an en France) qui survient dans 3 % des cas (soit 300 à 600 nouveaux cas/an en France dans les centres experts PulmoTension).


Le Pr Humbert a ensuite approfondi la 2e vision du RHU DESTINATION : le cheminement d’un patient ou care pathway :
- Détection : existent-ils des signes d’alerte/éléments au scanner initial chez un patient qui fait une embolie pulmonaire pour détecter l’HTP ?
- Référencement vers les centres experts : segmentation automatique des vaisseaux pulmonaires, bonne connaissance de la perfusion pulmonaire pour les déboucher de manière préférentielle…
- Traitements : faut-il traiter avant de désobstruer ? Existe-t-il un risque différent selon le degré d’obstruction/ la pression initiale ?
- Suivi des patients : outils d’imagerie et ingénierie pour savoir si certains patients ne récidivent pas et si l’hypertension pulmonaire persiste.
Hugo Pasquier, ingénieur GE HealthCare, Buc, a présenté les besoins cliniques des équipes de Bicêtre et de Marie-Lannelongue, sur les différents aspects du parcours patients pour y répondre d’un point de vue industriel.

Les tâches 1.2 et 1.4 s’intéressaient à la détection des signes radiologiques, soit lorsque la maladie est avérée, pour caractériser au mieux (1.2) l’ensemble des signes radiologiques pour prendre la bonne décision thérapeutique, soit pour intercepter la maladie au plus tôt (1.4).
Sur un scanner pulmonaire avec injection de contraste, il existe beaucoup de signes radiologiques divers c’est donc la ressource idéale pour développer des logiciels d’intelligence artificielle qui détectent, apprennent les signes radiologiques présents mais parfois peu connus des non experts.
- 1re partie, tâche 1.2 : caractérisation de la maladie avec des outils spécifiques d’annotation/labellisation d’images. Sur 170 examens, près de 6000 signes radiologiques ont été identifiés par les radiologues et pneumologues soit une moyenne de 35 lésions par examen avec une bonne exhaustivité des signes radiologiques rencontrés en pratique clinique. Le modèle a pu être entrainé pour détecter les signes qui pourraient être pathologiques. La sensibilité et spécificité sont bonnes (80 %) cependant sur des examens de contrôles, le modèle trouve aussi des lésions. Il faudrait donc pouvoir affiner le modèle (annotation, sensibilité) pour améliorer sa performance. Concernant les enjeux industriels, les 300 à 600 examens/an (cf. présentation du Pr Humbert) sont réalisés dans les 29 centres de l’hypertension pulmonaire – PulmoTension. Ainsi, la valeur du produit est faible comparativement au coût de développement d’un tel algorithme (validation clinique, conformité, etc.).
- 2e partie, tâche 1.4 : intercepter la maladie pour tenter de réduire le temps médian de diagnostic (14 mois) grâce à 50 examens réalisés au moment de l’épisode aigu d’embolie pulmonaire pour lesquels des signes de la maladie chronique sont présents. Le faible effectif rend difficile l’entrainement d’un modèle. Ainsi, ont été ajoutées des données publiques d’embolie pulmonaire aiguë (EPA) pour bien identifier les signes chroniques sur des examens aigus. Concernant les enjeux industriels, en France, l’EPA concerne 35000 examens/an dans 600 services d’urgence en général. Ainsi, comparativement au coût de développement, ce produit d’intelligence artificielle pourrait être adressé à de plus nombreux centres et aurait ainsi plus de valeur. Par ailleurs, les signes radiologiques à détecter pour l’interception de la maladie sont les mêmes que 14 mois plus tard, quand le diagnostic est posé (phase 1.2). L’entrainement du modèle avec des examens d’HTP-TEC pourrait donc permettre également d’intercepter les patients potentiellement à risque et les prendre en charge plus rapidement.
Les tâches ont donc été fusionnées pour aboutir à un unique modèle qui permettrait de caractériser la maladie (1.2) et de l’intercepter au moment de l’EPA, avec des signaux d’alarme (1.4). Le projet se poursuit actuellement.

En conclusion, la détection et caractérisation des signes radiologiques de l’HTP-TEC est une chose difficile même pour une IA. Pour une performance raisonnable et acceptable, les données mises à disposition doivent être en quantité et qualité suffisantes. D’un point de vue industriel, adresser l’ensemble du parcours patient, de nombreux centres, l’interception de la maladie, a plus de valeur. Enfin, il faut penser au modèle médico-économique pour financer ces solutions (développement, installation, utilisation).
Le Dr Mitja Jevnikar, pneumologue au centre de référence coordonnateur de l’hypertension pulmonaire – PulmoTension, hôpital Bicêtre, a abordé la nécessité de se comprendre, de discuter collégialement pour la détection et la prise en charge multidisciplinaire de l’HTP-TEC, pathologie rare et complexe.
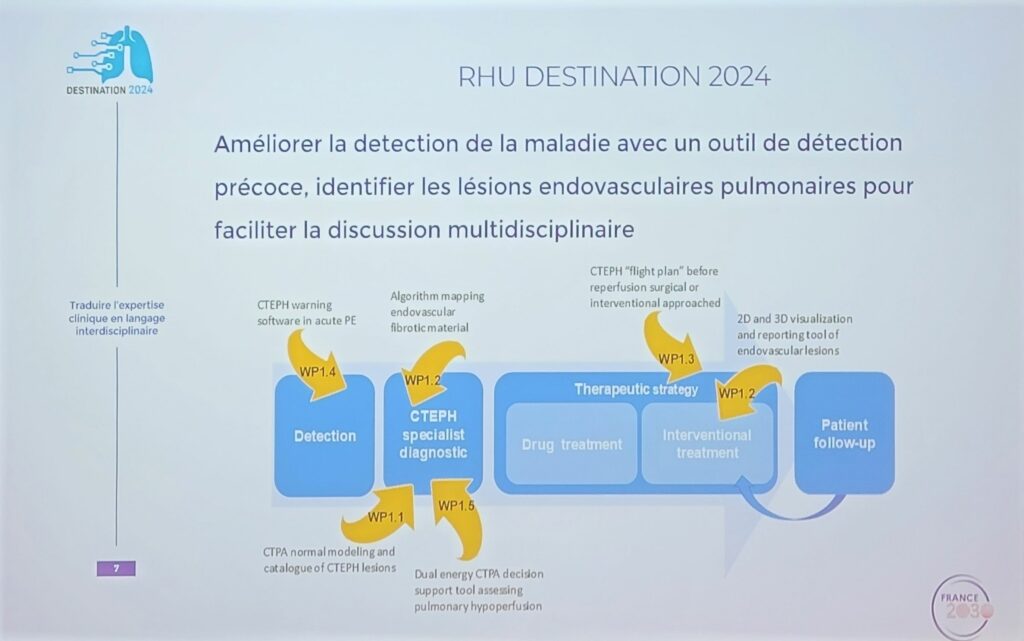
Le RHU DESTINATION a voulu se concentrer sur la détection de la maladie plus précoce et le mapping (cartographie) des lésions dans les vaisseaux. Les interprétations cliniques peuvent être différentes d’où la nécessité d’une discussion pluridisciplinaire.
Comment procéder ? Les cliniciens doivent voir et annoter les images avec des tags (balises) pour lesquelles les ingénieurs doivent développer des algorithmes pour aboutir à un outil de détection automatique des lésions.
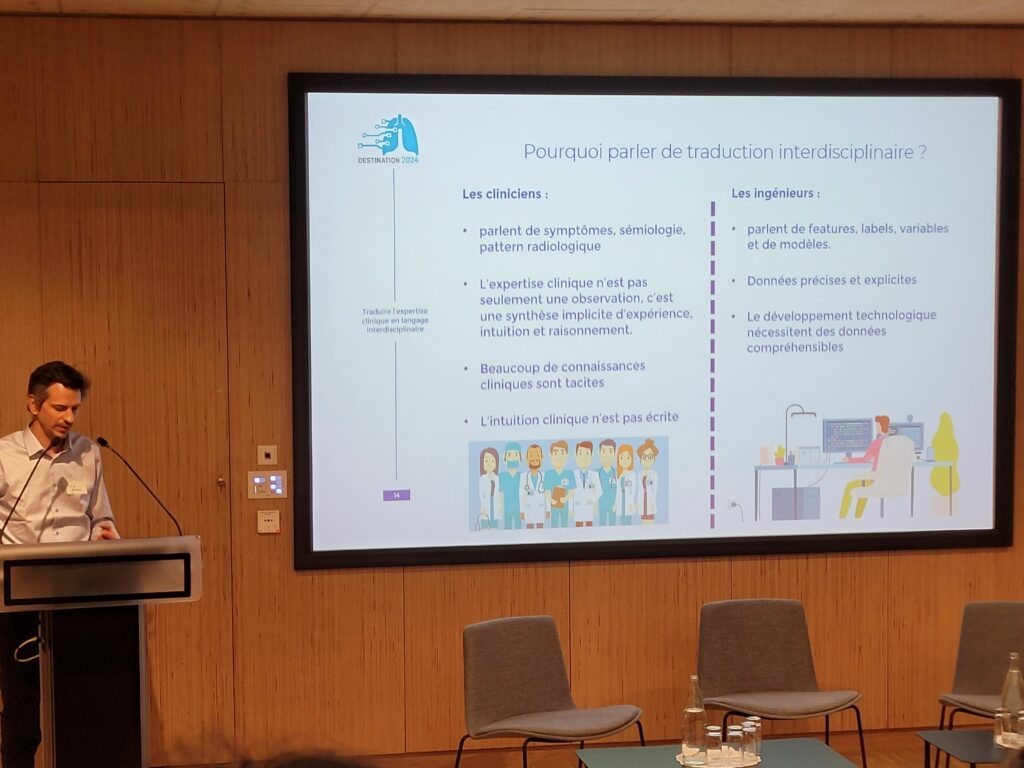
Ces tâches nécessitent plusieurs acteurs donc une équipe hybride : cliniciens de centres experts – pneumologues, radiologues, pharmaciens – techniciens qui parlent de symptômes, pattern (motifs) radiologiques et de l’autre côté des ingénieurs, data scientists, experts IA qui parlent de variables, de modèles, qui ne connaissent pas cette malade, qui ne l’ont jamais étudiée. Sans traduction, ces acteurs ne peuvent pas se comprendre.
Le Dr Jevnikar a ensuite explicité le processus d’annotation clinique, précis, avec caractérisation anatomique et des critères de sureté (coefficient de confiance) pour traduire l’expertise et l’intuition clinique en langage interdisciplinaire, explicite et, affiner l’outil en code informatique. Il a conclu en rappelant la nécessité de se (re)voir régulièrement pour expliquer ce qui est fait et ainsi pour s’améliorer collectivement en continu.
Le Pr Olaf Mercier, chirurgien thoracique au centre de référence constitutif de l’hypertension pulmonaire – PulmoTension, hôpital Marie-Lannelongue, a présenté le modèle animal qui vise à reproduire la maladie par certaines caractéristiques morphologiques : obstruction vasculaires pulmonaires, hypervascularisation systémique ou bronchique car lorsque une artère est obstruée de façon chronique, le poumon est revascularisé par les artères systémiques.
Chez certains patients, la gravité hémodynamique (augmentation des résistances vasculaires pulmonaires) n’est pas liée à la sévérité de l’obstruction proximale (artères bouchées). Ils ont ainsi voulu caractériser, reproduire l’atteinte microvasculaire (encore appelée vasculopathie pulmonaire distale) dans les territoires non obstrués. Il existe également des atteintes dans les territoires en aval de l’obstruction donc les artères reperfusées ne sont pas normales.
Le modèle animal de physiopathologie de la maladie est produit sur 6 semaines en liant l’artère pulmonaire gauche (= occlusion du poumon gauche) puis en embolisant chaque semaine dans le lobe inférieur du poumon droit pour augmenter petit à petit les pressions pulmonaires, amener un remodelage du ventricule droit (épaississement) et amener l’animal à des pressions pulmonaires qui sont la définition humaine de l’hypertension pulmonaire. Cela permet ainsi d’étudier la maladie chronique.

La difficulté est d’avoir une homogénéité de sévérité chez l’ensemble des animaux pour analyser les lésions observées mais cela permet des analyses en fonction de cette sévérité.
Le modèle est réversible par reperfusion pulmonaire gauche qui va reproduire une endartériectomie que l’on ne peut pas pratiquer car cela serait trop coûteux et technique.
Le Dr Xavier Jaïs, pneumologue au centre de référence coordonnateur de l’hypertension pulmonaire – PulmoTension, hôpital Bicêtre, aborde les aspects de la recherche clinique et notamment les difficultés rencontrées ainsi que les ajustements des pratiques pour aboutir aux objectifs de recrutement de l’étude IMPACT-CTEPH.

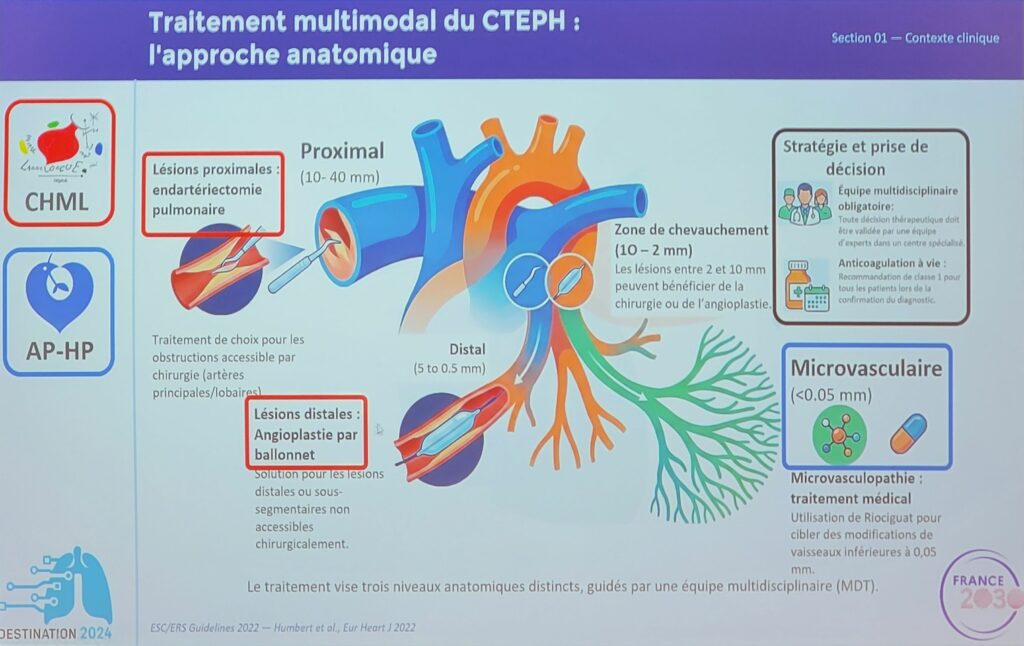
Pour rappel, les traitements de l’HTP-TEC ciblent la présence de caillots dans les artères de gros calibre des poumons ainsi que le remodelage des petits vaisseaux (artères < 0,5 mm). L’étude s’intéresse aux formes inopérables qui concerne 40 % des patients.
Pour les patients atteints d’hypertension pulmonaire thromboembolique chronique, inéligibles à une endartériectomie pulmonaire, avec le même niveau de preuves, les recommandations de traitement pour l’HTP-TEC étaient soit l’angioplastie pulmonaire (désobstrue le vaisseau) soit le traitement médicamenteux de référence (riociguat qui cible le remodelage). Au lancement du RHU, il n’existait pas d’étude sur l’association de traitements par contre, nous savions que l’angioplastie pulmonaire pouvait se compliquer avec des saignements autour des vaisseaux dilatés liés à la sévérité hémodynamique. L’étude RACE avait montré que traiter médicalement les patients par riociguat permettait d’améliorer l’hémodynamique des patients pour faire baisser la pression, les résistances et ainsi de diminuer les complications résultant de l’angioplastie pulmonaire.
À la lumière de ces éléments, l’étude de stratégie IMPACT-CTEPH, en collaboration avec le laboratoire Janssen, a été élaborée et ouverte à tous les centres français labellisés de l’hypertension pulmonaire – PulmoTension. Elle a comparé l’efficacité et la sécurité d’emploi de la bithérapie (riociguat et macitentan) versus la monothérapie de référence (riociguat seul) avant une angioplastie pulmonaire afin de déterminer si une combinaison thérapeutique en amont peut davantage diminuer les complications de l’angioplastie pulmonaire. Le critère de jugement principal était la modification des résistances vasculaires pulmonaires.
La problématique de cette étude était la sélection des patients inopérables qui repose sur une réunion de concertation pluridisciplinaire (RCP) hebdomadaire qui associe les équipes de Bicêtre et de Marie-Lannelongue. Il fallait donc réunir l’ensemble des acteurs pour savoir si les lésions étaient accessibles en angioplastie pulmonaire, réunir l’ensemble des résultats, réunir une imagerie de très haute qualité cela généralement par envois de courriers puis ensuite adresser les conclusions de cette RCP. Ce processus complexe, peu agile, a débuté en 2021 pendant la crise covid ce qui a été un frein à l’inclusion des malades. Une fiche type a ainsi été diffusée aux centres pour harmoniser les pratiques et en parallèle l’assouplissement du critère d’inclusion lié au cathétérisme cardiaque droit a été validé. Une première prolongation a été obtenue avec une période d’inclusion initiale qui est passée de 24 à 30 mois (fin déc. 2023). Ces premiers ajustements ont permis une nette amélioration de l’inclusion sans toutefois atteindre l’objectif théorique.
Pour une imagerie homogène, de haute qualité, avec Le Pr Olivier Meyrignac, radiologue, hôpital Bicêtre, un protocole optimisé de double acquisition d’imagerie thoracique a été diffusé : précoce, elle permet une bonne visualisation des artères pulmonaires et, tardive, une bonne visualisation des vaisseaux systémiques. En parallèle, le parcours s’est fluidifié grâce aux évolutions technologiques (partage d’imagerie PACS, visioconférence). Une ultime prolongation de 36 à 42 mois a permis d’atteindre les objectifs d’inclusion de l’étude.

« Il a fallu être très souple, avec un pilotage pragmatique, et être capable de s’adapter à toutes les circonstances. »
Le Dr Christophe Guignabert, directeur de recherche, UMR S 1358, Inserm, a montré comment les prolongations ont permis de transformer les objectifs et les retombées scientifiques du 2e groupe de travail dédié aux mécanismes physiopathologiques des atteintes microvasculaires pulmonaires. Ces prolongations ont été un accélérateur pour mieux comprendre en profondeur ces mécanismes et également pour aller au-delà des objectifs initiaux (2021) : comprendre si le développement de l’HTP-TEC était associée ou non aux modifications des 3 grandes voies thérapeutiques de l’hypertension pulmonaire :
- voie de l’endothéline qui est un puissant vasoconstricteur ;
- voie vasodilatatrice du monoxyde d’azote ;
- voie vasodilatatrice de la prostacycline.
Durant ces 30 dernières années, une innovation sans précédent a concerné ces 3 voies avec le développement de nombreux médicaments qui permettent de restaurer à la normale les signalisations de ces trois voies thérapeutiques cependant ces médicaments ne sont approuvés pour l’HTP-TEC. Le laboratoire a eu accès aux tissus pulmonaires, extrêmement rares et précieux, de 10 patients opérés à Marie-Lannelongue qui ont pu montrer que la balance entre les vasoconstricteurs et les vasodilatateurs était perturbée en faveur de la vasoconstriction.
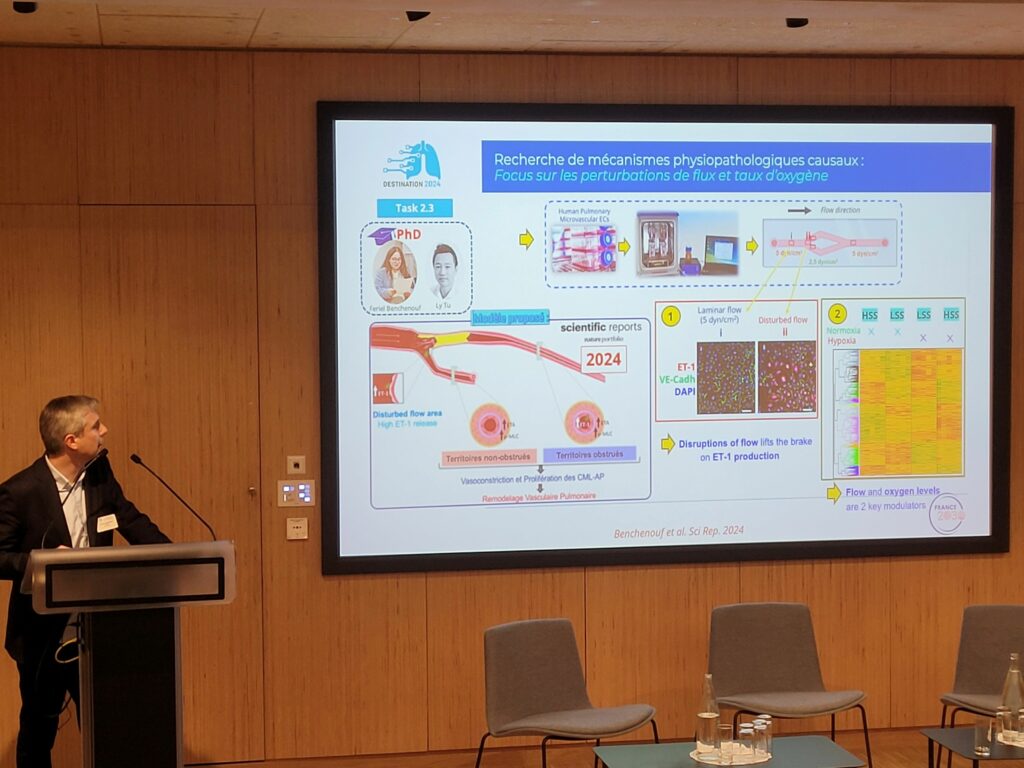
En parallèle, avec Feriel Benchenouf, les perturbations du flux sanguin et les variations du taux d’oxygène ont été étudiées sur des cellules endothéliales. Un modèle mécanistique a pu être proposé pour l’HTP-TEC : l’obstruction entraine des perturbations de flux et lève le frein de production de l’endothéline 1 qui va aller circuler et signaler en aval, dans les petites artères pulmonaires, en se posant sur son récepteur pulmonaire ET1, surexprimé dans la maladie, qui va installer un cercle vicieux qui va promouvoir la vasoconstriction et sur le long terme une une prolifération et une microvasculopathie qui va se mettre en place.
Mais quels sont les gènes et les voies de signalisation importants pour l’adaptation ou la mal-adaptation des cellules endothéliales d’une manière générale ? Grâce aux prolongations, il a été possible de répondre clairement à ces questions. Les cellules endothéliales exposées à du flux, sous hypoxie, réduisent leur allongement et l’alignement entre le noyau et l’appareil de Golgi est perturbé. Ainsi, l’hypoxie empêche l’adaptation mécanique de l’endothélium pulmonaire lorsque le flux est élevé. Ces altérations sont associées à des modifications transcriptomiques dont une extinction des voies TNF et TGFβ sous hypoxie.
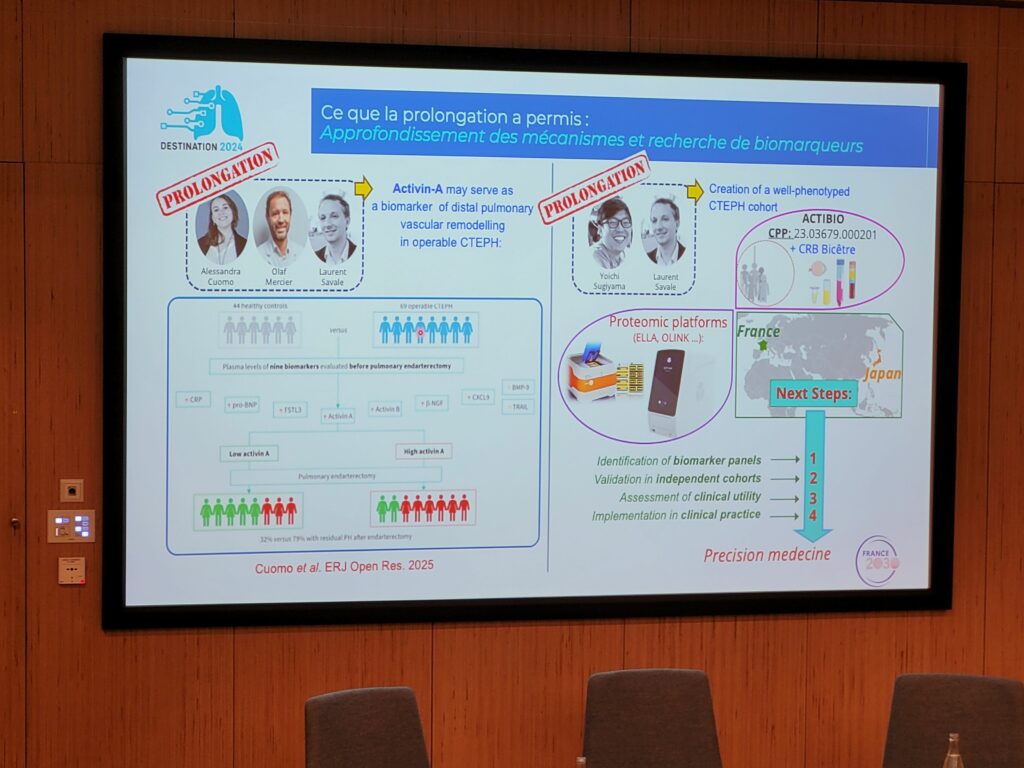
Est-ce que le facteur PlGF, l’inflammation sont présents dans l’HTP-TEC ? Peut-on prédire la microvasculopathie ? Il a été possible de doser les facteurs inflammatoires et les ligands de la voie TGFβ (vue comme altérée dans la pathologie) dans des échantillons de patients atteints d’HTP-TEC avant et après chirurgie grâce au Pr Olaf Mercier. Les résultats d’Alessandra Cuomo, présentés par le Pr Laurent Savale montrent l’importance de suivre les protéines circulantes dans le sang des patients.
Le projet se poursuit avec une biobanque ouverte en 2023 dans le centre dé référence. L’objectif est de collecter tous les échantillons possibles de patients avec pour objectif d’aller vers la médecine de précision et le traitement personnalisé. L’idée est d’utiliser les échantillons sélectionnés, très phénotypés, pour rechercher des biomarqueurs de sévérité de la maladie en les validant dans des cohortes indépendants et grâce au Pr Yoichi Sugiyama cela débutera au Japon.
Le Pr Laurent Savale, pneumologue au centre de référence coordonnateur de l’hypertension pulmonaire – PulmoTension, hôpital Bicêtre, a conduit sa présentation dans la suite de celle de Christophe Guignabert, en abordant plus en détails les biomarqueurs et leur intérêt dans l’HTP-TEC.
Il a rappelé que parallèlement au lancement du RHU, la voie TGFβ montrait son intérêt thérapeutique dans l’HTAP (groupe 1) avec un dysfonctionnement de la voie BMPR2 mais également par une suractivité de la voie activine (phosphorylation smad2/3, augmentation de la production des ligands et des récepteurs au niveau des cellules endothéliales et des cellules musculaires lisses) qui participe au remodelage vasculaire pulmonaire. Cela se traduit également par une modification des biomarqueurs circulants de la voie activine dont certains sont modulés avec l’introduction de traitements spécifiques de l’HTP. Ils peuvent donc avoir un intérêt dans la stratification pronostique des patients. Le sotatercept permet de cibler cette hyperactivité de la voie activine avec une efficacité pour le groupe 1. L’arrivée de ces nouvelles thérapies incitent à aller vers une médecine de précision pour pouvoir identifier les patients qui pourraient être bénéficiaires de ces thérapies ciblées et pour essayer également de prédire les effets secondaires. Ce sont également les objectifs de la FHU Cournand.
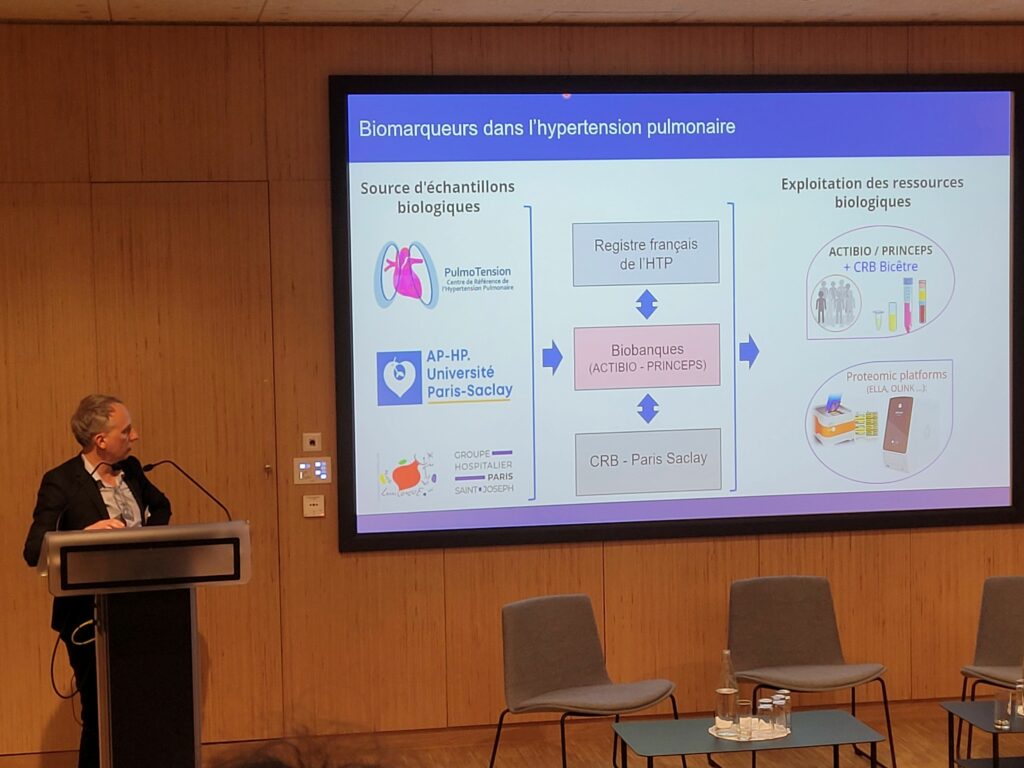
Pour mener ces recherches, il existe le registre français de l’hypertension pulmonaire mais aussi des biobanques en lien avec le CRB de Paris-Saclay :
- ACTI-BIO, 2023, Bicêtre, 1200 patients atteints de toutes formes d’HTP
- PRINCEPS, Marie-Lannelongue sous la gouvernance d’Olaf Mercier, patients HTP-TEC et transplantés.
Les travaux de protéomique peuvent être mené grâce à la technologie présente dans l’unité Inserm UMR S 1358.
Trois objectifs des biomarqueurs :
- améliorer la détection précoce
- prédire la survenue d’événements cliniques (travaux existant depuis 20 ans dans l’HTAP)
- prédire la réponse au traitement pour aller vers une médecine de précision. L’HTP-TEC se prête bien à cela pour identifier ce qui est lié à la microvasculopathie et ce qui est lié à l’obstruction justement pour prédire la réponse au traitement de désobstruction.
La voie de TGFβ a été très peu étudiée dans cette forme d’hypertension pulmonaire. L’idée est de voir si cette voie peut être impliquée dans la microvasculopathie et si, comme pour l’HTAP, il est possible de reproduire un intérêt pour les biomarqueurs circulants qui couvrent cette voie de signalisation et si elle peut prédire la réponse à la désobstruction c’est à dire être un marqueur indirect de la microvasculopathie non traitée directement par la désobstruction.
L’étude préliminaire a été menée dans une cohorte exploratoire de patients HTP-TEC et patients contrôles puis de patients HTP-TEC transplantés. Les résultats montrent des marqueurs d’inflammation augmentés (CRP), ainsi que d’activine A et B et FSTL3 (inhibiteur de la voie).
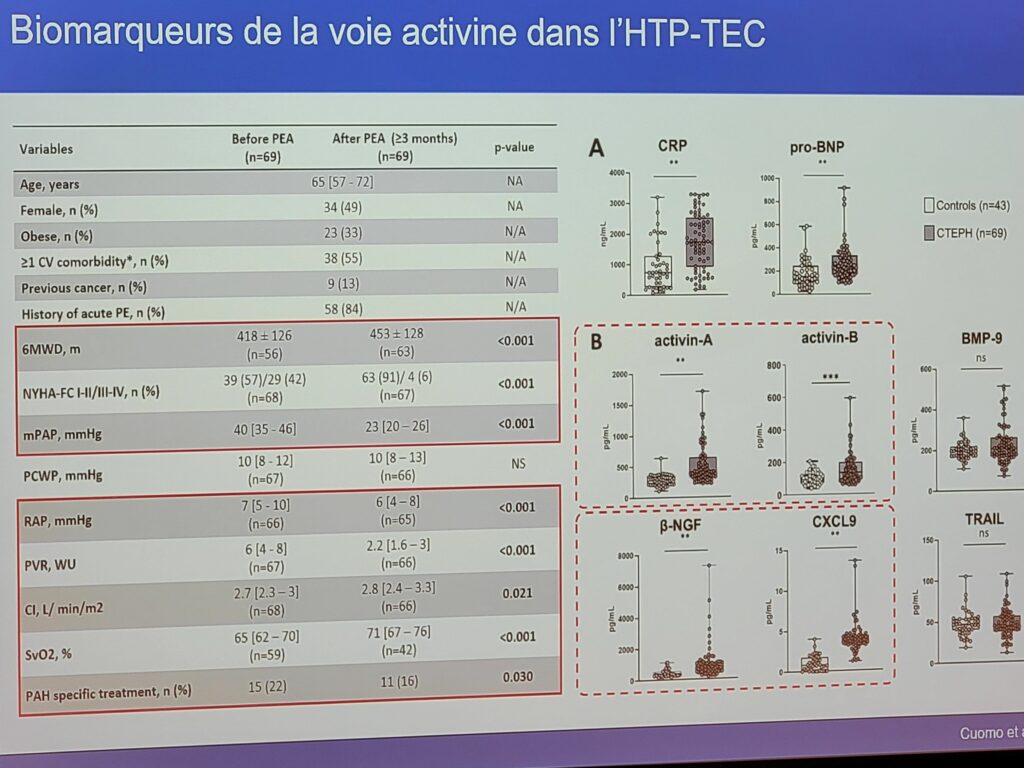
Est-ce que ces biomarqueurs et hémodynamiques sont prédictifs d’une hypertension pulmonaire résiduelle ? Les valeurs hémodynamiques (niveau de pression), la CRP sont retrouvées tout comme l’activine A et le FSTL3 qui sont associés à un risque augmenté d’avoir une HTP résiduelle. En combinant ces données aux données histologiques, ces biomarqueurs pourraient être représentatifs de la microvasculopathie chez les patients ayant une obstruction du lit vasculaire pulmonaire.
L’objectif est à présent de mener :
- une étude exploratoire et une étude de validation en partenariat avec l’équipe japonaise qui dispose une biobanque HTP-TEC ;
- d’élargir à des formes non opérables, accessibles qu’en angioplastie pulmonaire donc à des formes plus distales ;
- d’intégrer ces biomarqueurs dans une étude multiparamétrique qui pourrait intégrer des analyses d’imageries beaucoup plus fines sur des analyses hémodynamiques, fonctionnelles.
Le Pr Olivier Meyrignac, radiologue au centre de référence coordonnateur de l’hypertension pulmonaire – PulmoTension, hôpital Bicêtre, a présenté sa formation à l’angioplastie pulmonaire par ballonnet (APB).

Il a rappelé le contexte clinique avec :
- la chirurgie, l’endartériectomie pulmonaire qui est le gold standard (la référence)
- les traitements médicamenteux dont Bicêtre est un pôle de référence mondial pour le développement, son implémentation dans les recommandations
- l’angioplastie pulmonaires par ballonnet qui est la dernière brique ajoutée à l’arsenal thérapeutique. Il était donc très important de la maitriser à Bicêtre en plus de Marie-Lannelongue.
Il a ensuite précisé le rôle de la radiologie dans l’HTP-TEC, qui faute de soigner les patients (hormis angioplastie) est central dans la prise en charge diagnostique par l’observation sur le cathétérisme cardiaque droit, de thrombus, sténoses, occlusions, signes indirects, etc. qui vont permettre d’affirmer le diagnostic d’HTP-TEC, de faire une cartographie lésionnelle et vont orienter la prise en charge soit vers la chirurgie soit vers l’APB.
Pourquoi se former à l’APB ? Car elle est efficace, réduit les résistances vasculaires pulmonaires, la pression artérielle pulmonaire moyenne, augmente la qualité de vie des patients avec leur périmètre de marche et a un effet positif sur la survie. Cependant, l’étude RACE a montré que la technique est délicate et dangereuse avec des œdèmes de reperfusion, des hémoptysies par perforation vasculaire ainsi que des défaillances hémodynamiques secondaires au traitement. Il existe une courbe d’apprentissage documentée de cette technique. Au delà de 200 procédures d’ABP, 50 patients/opérateur/an, on est considéré comme un expert et cela diminue les complications.
L’APB a commencé en 1988 mais a pris de l’ampleur avec les bonnes pratiques japonaises du centre de référence Okayama, qui ont diffusé dans les années 2000-2010 notamment par la formation de l’expert, le Pr Yoichi Sugiyama qui a fait 18 mois de compagnonnage, au lit du patient, à l’hôpital Bicêtre pour former les personnels et partager ses connaissances. Ainsi, le site de Bicêtre regroupait tous les éléments pour permettre d’acquérir l’APB.
L’apprentissage s’est déroulé en plusieurs phases :
- procédures théoriques : bases, classification lésionnelle, sélection des lésions, gestion des complications, revue des cas en pré-opératoires
- phase de démonstrations complètes essentiellement à Marie-Lannelongue avec justification des actes, décisions, protocoles de sécurité, explications au manipulateur d’électroradiologie, en pneumologie pour la surveillance ainsi qu’au réanimateur
- transfert progressif sur le geste avec une prise de responsabilité croissante, une assistance rapprochée puis partielle avec une présence de chacune des décisions critiques
- pour finir avec une supervision externe (hors salle) avec un debriefing post-procédure pour améliorer les pratiques. Cela a permis de rédiger près de 70 protocoles notamment pour la gestion des complications (< 3 %).
Cinq radiologues ont pu être formés ainsi que dix manipulateurs en électroradiologie à l’AP-HP. Les retombées sont donc importantes pour le service qui vise à avoir une double compétence : diagnostic et interventionnelle. Il existe ainsi un retour d’expérience inversé de l’interventionnel vers le diagnostic qui intègre davantage le radiologue dans le diagnostic de l’HTP-TEC. Les pratiques japonaises diffèrent de celles de Marie-Lannelongue, c’est donc un enrichissement des pratiques.
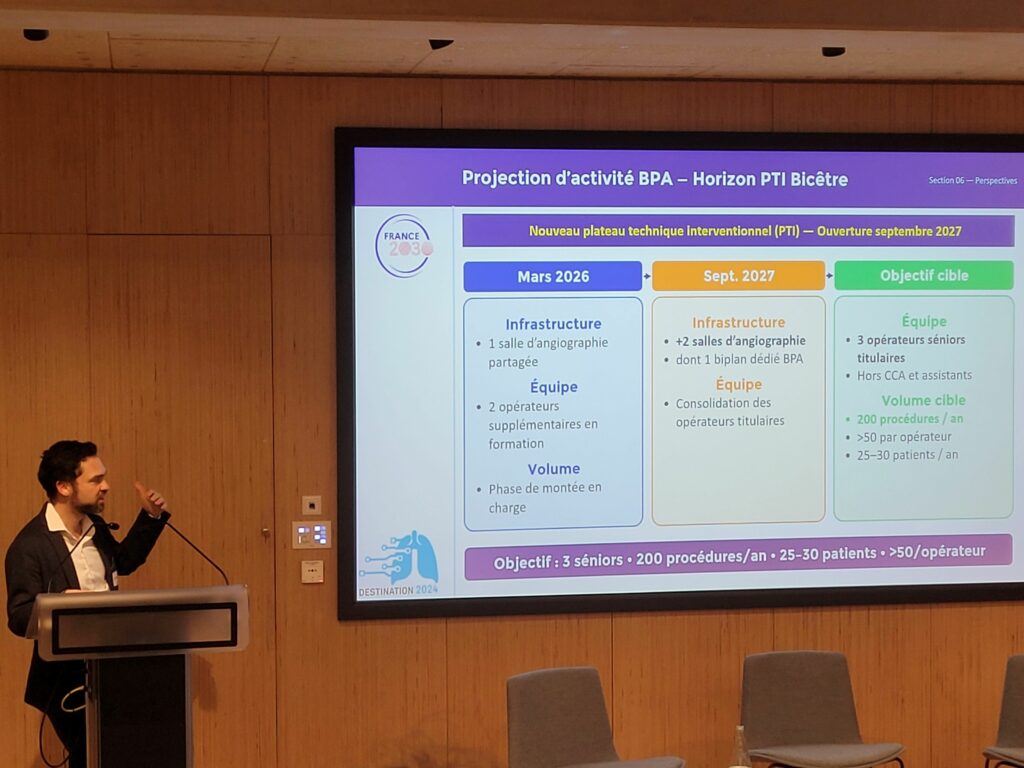
Les perspectives sont de monter en charge en terme de formation mais aussi de volume et, le nouveau plateau interventionnel en septembre 2027, avec 2 salles d’angiographie à Bicêtre permettra d’améliorer la qualité et la sécurité des procédures pour aboutir à 200 procédures/an soit 25 à 30 patients/opérateur.
Le Pr Yoichi Sugiyama, cardiologue au centre médical d’Okayama a présenté le potentiel de l’angioplastie pulmonaire par ballonnet qui se pratique dans 30 centres au Japon.

Initialement, la dilatation se faisait par étape, en 4 séances alors que la nouvelle stratégie vise beaucoup de segments en une seule étape.
Il conclut son propos en estimant que le centre de référence PulmoTension de Bicêtre dispose à présent de l’approche japonaise et a le potentiel pour devenir un centre éducatif grâce aux graines qu’il a semées pendant ce compagnonnage.
Le Pr Marc Humbert, responsable scientifique du RHU DESTINATION 2024, pour finir cet après-midi d’échanges a abordé les perspectives de l’après projet.

Le potentiel qui peut émerger de cette aventure collective avec 3 projets qui pourraient être une valeur ajoutée :
- la décroissance thérapeutique après rémission de l’HTP-TEC, PHRC DIRECTION animé par le Dr Mitja Jevnikar ;
- la vulnérabilité pulmonaire, les éléments de prévention (pollution, infection respiratoire, tabac, etc.) pour faire en sorte que la croissance pulmonaire et la santé respiratoire des enfants soient correctes. Un consortium d’IHU a été mis en place grâce au soutien financier QIM de la région IDF ;
- prévenir les maladies respiratoires et les intercepter (programme national de recherche PrevAction, France 2030).
M. Nicolas Revel, directeur général de l’AP-HP, a conclu cette réunion de présentation des travaux scientifiques en saluant tout le bilan de ce RHU DESTINATION 2024 aux objectifs dépassés et cet après-midi qui aura permis de rebalayer ces 6 années de travail, de collaboration, d’ajustement, de réussite, d’engagement, d’aventure collective dans la durée pour évoluer, rater, progresser, confronter des approches, dépasser des frontières disciplinaires, institutionnelles, en réunissant des univers différents.

« Les RHU permettent aussi de faire dialoguer la recherche fondamentale, l’innovation technologique, la clinique, l’organisation des soins, le développement des compétences professionnelles, dans une dynamique collective et intégrée.
Dès l’origine le RHU DESTINATION s’est fixé des objectifs ambitieux et 6 années plus tard, les résultats sont impressionnants !
Le RHU est une affaire d’équipes, de partenaires, qui ont tous su travailler en co-construction et qui permet le rayonnement même du projet. »
M. Revel a rendu hommage au leader scientifique, le Pr Marc Humbert, au delà de son expertise scientifique, pour son engagement, sa vision, sa capacité à fédérer les équipes et à faire vivre ce collectif dans la durée. Ce travail renvoie également à différents personnels dans la diversité des compétences et des métiers et il les saluent toutes et tous !
Il conclut son propos en insistant sur la magnifique démonstration de la force du modèle sous-jacent des RHU : travail en proximité des acteurs différents, assurer le continuum de la recherche jusqu’au soin, associer la dynamique du public et du privé, s’inscrire dans des cadres souples et qui ont le temps.
Cette rencontre a illustré la manière dont un travail de proximité entre recherche fondamentale, innovation technologique et pratique clinique a permis de faire émerger des avancées concrètes au service des patients atteints d’HTP-TEC. Le RHU DESTINATION 2024 est la preuve que le succès d’un projet médico-scientifique repose grandement sur le collectif, sa capacité d’adaptation et son engagement au delà des difficultés inhérentes à tout projet.


